1. (UFRGS) O calor específico da água é
de 1,0 cal/gºC. Para que a temperatura de uma amostra de 20 g de água varie de 20ºC para 50ºC, ela deve absorver
(A) 0,7 cal
(B) 20 cal
(C) 200 cal
(D) 600 cal
(E) 1.000 cal
2. (UFRGS) Um gás é aquecido dentro de um
recipiente de volume constante. Nessas condições,
(A) aumenta a energia cinética média de translação
das moléculas do gás.
(B) é realizado um trabalho pelo gás.
(C) a pressão do gás diminui.
(D) a pressão do gás permanece constante.
(E) ocorre uma transformação adiabática.
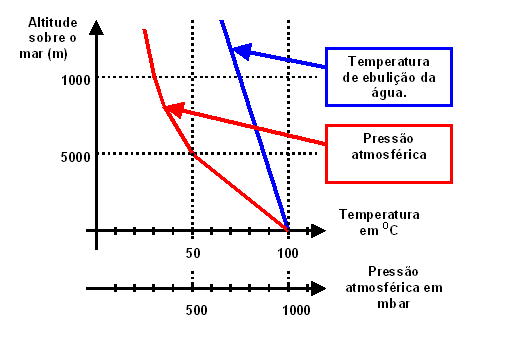
3. (UFRGS) O gráfico representa as variações
da pressão atmosférica e da temperatura de ebulição da água, ambas em função da
altitude acima do nível do mar.
Das afirmações seguintes,
I - Para a temperatura de ebulição da água
variar, em função da altitude, na forma indicada no gráfico, é necessário que a
água se encontre em um recipiente aberto.
II - Em função da altitude, a pressão atmosférica
cai mais rapidamente à metade do valor que possui ao nível do mar do que o
ponto de ebulição da água.
III - Qualquer que seja a altitude considerada, a
variação percentual da pressão atmosférica é maior do que a correspondente
variação percentual do ponto de ebulição da água.
quais as que se aplicam corretamente a esta
situação?
(A) Apenas I
(B) Apenas II
(C) Apenas III
(D) Apenas I e II
(E) I, II e III
4. (UFRGS) Mistura-se gelo a 0ºC com água
quente em um recipiente termicamente isolado. O balanço de energia é o
seguinte: 356 J/g são cedidos pela água quente, ao passo que 335 J/g são
absorvidos para fusão do gelo. Considerando o calor específico da água 4,2
J/g.K, qual é a temperatura de equilíbrio da mistura?
(A) 0ºC
(B) 0,5ºC
(C) 5ºC
(D) 21ºC
(E) 88,2ºC
5. (UFRGS) Um ebulidor cede energia a 100 g de água a uma taxa constante em relação ao tempo. Para elevar a temperatura de cada grama de
água de 15ºC a 100ºC, são necessários 360 J de energia. Sabendo-se que para
evaporar completamente as 100 g de água, após atingidos os 100ºC, transcorre
seis vezes mais tempo do que para elevar sua temperatura de 15ºC a 100ºC, o
calor de vaporização da água pode ser estimado em
(A)
60 J/g
(B)
480 J/g
(C)
600 J/g
(D) 1.800 J/g
(E) 2.160 J/g
6. (UFRGS) Cede-se a um sistema, constituído
por um gás contido em um recipiente, 20 J de energia na forma de trabalho e 15
J na forma de calor. Qual é a variação da energia interna desse sistema?
(A) 35 J
(B) 20 J
(C) 15 J
(D) 5 J
(E) zero
7. (UFRGS) Quantos gramas de água a 10ºC
deve-se misturar com 200 g de água a 85ºC para que a temperatura final da
mistura seja de 40ºC?
(A) 133
(B) 200
(C) 225
(D) 300
(E) 425
8. (UFRGS) Selecione a alternativa que
completa corretamente as lacunas do período seguinte:
Um gás sofre uma transformação isovolumétrica
quando recebe uma quantidade de calor Q. Nessa transformação termodinâmica, a
temperatura final do gás é ...... inicial, e o trabalho realizado é ...... .
(A) menor do que a - diferente de zero
(B) maior do que a - diferente de zero
(C) igual à - diferente de zero
(D) maior do que a - nulo
(E) menor do que a - nulo
9. (UFRGS) A posição l da extremidade da coluna de líquido de um
termômetro varia de acordo com a função
![]()
De quanto varia a posição da extremidade da coluna
de líquido quando a temperatura T(oC) varia de -10oC a
110oC?
(A) 110 mm
(B) 120 mm
(C) 200 mm
(D) 220 mm
(E) 240 mm
10. (UFRGS) Um bloco de gelo,
a temperatura não determinada, recebe uma quantidade não especificada de calor.
Nessas condições ocorre necessariamente uma mudança
(A) na temperatura do bloco de gelo.
(B) de estado
(C) na energia interna do bloco de gelo.
(D) no calor específico do gelo.
(E) na capacidade térmica do bloco de
gelo.
11. (UFRGS)
Considere as seguintes afirmações:
I - É possível aumentar a temperatura de um gás
sem que necessariamente ele se encontre em contato com uma fonte de calor.
II - Aumentando-se a energia cinética média das
moléculas de um gás, aumenta sua temperatura.
III - Numa máquina térmica, o calor cedido a um
gás pode apenas em parte ser usado para realizar trabalho.
Quais estão corretas?
(A) Apenas II
(B) Apenas III
(C) Apenas I e II
(D) Apenas II e III
(E) I, II e III
12. (UFRGS) Selecione a
alternativa que completa corretamente as lacunas nas afirmações seguintes:
I - Num dia quente, os fios elétricos entre dois
postes de luz encurvam-se ...... do que num dia frio.
II - Para aumentar de 20o C a
temperatura de 1,0 kg de ferro, é necessário ...... calor do que para aumentar,
também de 20o C, igual quantidade de massa de água, estando ambos a
uma temperatura inicial de 15o C.
III - Uma panela de ferro escura esfria ......
rapidamente do que uma panela de ferro clara, logo após terem sido retiradas
simultaneamente de um forno onde se encontravam aquecidas à mesma temperatura.
(A) menos - menos - mais
(B) menos - mais - menos
(C) mais - mais - menos
(D) mais - menos - menos
(E) mais - menos - mais
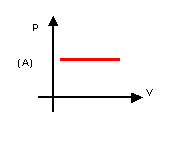
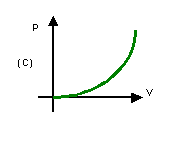
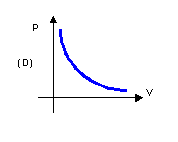
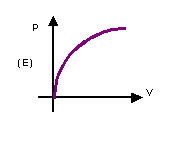
13. (UFRGS) A tabela mostra
algumas medidas de pressão (p) e volume (V) de um gás (O2), mantido
a temperatura constante. Qual o gráfico que melhor identifica a relação entre p
e V?

 |
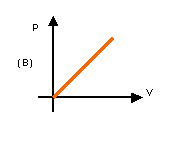 |
 |
 |
 |
14. (UFRGS) Certa massa m de
gelo à pressão atmosférica e inicialmente a uma temperatura de -16 oC,
requer uma energia de 320 J para sua temperatura elevar-se até 0 oC.
Para a fusão do gelo são necessários 3200 J e para a água resultante do gelo atingir
a temperatura de 80 oC são necessários mais 3200 J. De quanto é o
aumento da energia interna da massa m, em J ?
(A) 320
(B) 3200
(C) 3520
(D) 6400
(E) 6720
15. (UFRGS) Se o vácuo
existente entre as paredes de vidro de uma garrafa térmica fosse total,
propagar-se-ia calor de uma parede para a outra, apenas por
(A) convecção.
(B) radiação.
(C) condução.
(D) convecção e radiação.
(E) condução e convecção.
16. (UFRGS) O gráfico mostra
a variação de volume V de uma certa quantidade de água e do volume interno de
um recipiente de vidro que a contém, em função de suas temperaturas (T).
Supondo-se que a 4 oC o recipiente se encontre inteiramente cheio de
água, esta transbordará do recipiente, se a temperatura da água e a do
recipiente assumirem valores
(A) entre 0 oC e 4 oC,
apenas.
(B) acima de 4 oC,
apenas.
(C) abaixo de 0 oC,
apenas.
(D) acima de 10 oC,
apenas.
(E) ou acima ou abaixo de 4 oC.
17. (UFRGS) Um sólido homogêneo
apresenta a 5 °C um volume igual a 4,00 dm³. Aquecido até 505 °C, seu volume aumenta 0,06 dm³. Qual o coeficiente de dilatação linear aproximado do
material desse sólido?
(A) 3x10-5 °C-1
(B) 2x10-5 °C-1
(C) 1,5x10-5 °C-1
(D) 1x10-5 °C-1
(E)
0,5x10-5 °C-1
18. (UFRGS) Durante o aquecimento de um
litro de água de 20 °C a 60 °C, o que ocorre com o volume e a densidade dessa
água, respectivamente?
(A) permanece o mesmo - aumenta
(B) aumenta - diminui
(C) aumenta - aumenta
(D) diminui - aumenta
(E) diminui - diminui
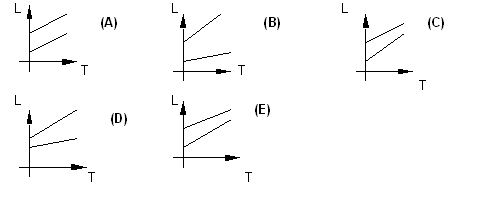
19. (UFRGS) As barras metálicas, X e Y,
têm o mesmo coeficiente de dilatação linear, positivo e constante para um certo
intervalo de temperatura, mas X é mais comprida do que Y. Analisando a
dilatação destas barras, qual o gráfico que melhor representa os comprimentos
(L) das mesmas em função da temperatura (T)?
20. (UFRGS) O gráfico representa a
variação da temperatura T em função da quantidade de calor Q fornecida aos
corpos X e Y. A massa de Y é igual ao dobro da massa de X. Com base nessas
informações, verifica-se que
(A) o calor específico de X é igual ao dobro do de
Y.
(B) o calor específico de X é menor do que o de Y.
(C) a capacidade térmica de X é igual ao dobro da
de Y.
(D) X e Y têm o mesmo calor específico.
(E) X e Y têm a mesma capacidade
térmica.
21. (UFRGS) Um gás se expande
adiabaticamente. Nessa transformação
(A) a energia interna do gás aumenta.
(B) a pressão do gás aumenta.
(C) há troca de calor com o meio externo.
(D) a temperatura do gás diminui.
(E) não há trabalho realizado pelo gás.
22. (UFRGS) Um corpo de 2 kg recebe 8000 J de calor e sofre uma variação de temperatura de 100 °C . O valor do calor específico desse corpo, em J/kg °C , é
(A) 40
(B) 80
(C) 160
(D) 4x105
(E) 8x103
23. (UFRGS) Numa escala termométrica
linear W, a temperatura de fusão do gelo é -70 oW, e a temperatura
de ebulição da água é 130 oW. A temperatura absoluta correspondente
ao 0 oW dessa escala é aproximadamente
(A) 35 K
(B) 135 K
(C) 238 K
(D) 273 K
(E) 308 K
24. (UFRGS) Cada um dos gráficos abaixo
mostra a relação entre as temperaturas de duas escalas termométricas X e C
(Celsius).

Quais os gráficos que melhor representam a relação
entre as temperaturas Kelvin e Celsius e entre as temperaturas Fahrenheit e
Celsius, respectivamente?
(A) 1 e 2
(B) 1 e 3
(C) 2 e 1
(D) 2 e 3
(E) 3 e 1
25. (UFRGS) Quando fornecemos 100 J de
calor a um gás ideal, esse realiza um trabalho conforme mostra o gráfico, indo
do estado i ao estado f.
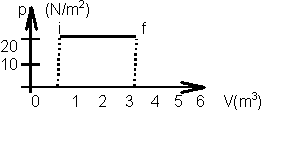
Qual a variação da energia interna do gás para essa
transformação?
(A) nula
(B) 20 J
(C) 80 J
(D) 100 J.
(E) 180 J
26. (UFRGS) Quando a temperatura
absoluta de uma amostra de gás ideal é duplicada, o módulo da velocidade média
de suas moléculas
(A) quadruplica.
(B) duplica.
(C) diminui de um fator ![]() .
.
(D) aumenta de um fator ![]() .
.
(E) permanece inalterada.
27. (UFRGS) A cada uma das situações
descritas (coluna da direita), associe o principal processo de transferência de
energia (coluna da esquerda) envolvido.

A relação numérica, de cima para baixo, da coluna da
direita, que estabelece a sequência de associações corretas é:
(A) 1 - 2
(B) 1 - 3
(C) 2 - 1
(D) 2 - 3
(E) 3 - 1
28. (UFRGS) O desenho mostra um
cilindro de metal dotado de um êmbolo móvel em cujo interior se encontra um gás
ideal em equilíbrio termodinâmico.
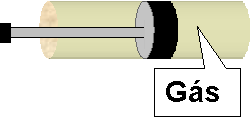 |
Em dado instante uma força de módulo F age sobre o
êmbolo que comprime o gás rapidamente. Durante a compressão
I - ocorre um aumento de energia interna do gás.
II - o trabalho realizado pela força de módulo F
produz uma elevação da temperatura do gás.
III - o trabalho realizado pela força de módulo F é
igual a quantidade de calor que se transmite para o meio externo.
Quais estão corretas?
(A) Apenas I
(B) Apenas II
(C) Apenas I e II
(D) Apenas II e III
(E) I, II e III
29. (UFRGS) As moléculas de um líquido
encontram-se em permanente agitação, movimentando-se em todas as direções, com
velocidades de módulos variados. Algumas das moléculas que atingem a superfície
do líquido, com valores de velocidade suficientemente altos, conseguem escapar
do seu interior. Considerando que são as moléculas de maior velocidade que escapam
do líquido e que as de menor velocidade nele permanecem, a energia cinética
média das moléculas do líquido diminui, o que representa um decréscimo da sua
temperatura. O número de moléculas que escapa por unidade de tempo depende de
fatores como a temperatura do líquido, a área de sua superfície livre e a
ventilação nas proximidades dessa superfície.
O texto acima refere-se ao fenômeno de
(A) evaporação.
(B) sublimação.
(C) fusão.
(D) condensação.
(E) solidificação.
30. (UFRGS) O gráfico mostra a relação
entre as temperaturas que registram dois termômetros, um em escala °C (Celsius)
e outro em °X , quando a pressão é de 1 atm. Essa relação mantém-se para
temperaturas entre -50 °C e 200 °C. Para que temperatura em °X ocorre a
ebulição da água a 1 atm?
(A) 25 °X
(B) 100 °X
(C) 192 °X
(D) 275 °X
(E) 333 °X
31. (UFRGS) A tabela mostra o ponto de
fusão (P. F.) e o calor latente de fusão (C. L.) de algumas substâncias à
pressão de 1 atm.

Com base nesses dados são feitas as seguintes
afirmações:
I - Para a pressão dada, a temperatura na qual
ocorre a fusão é bem determinada para cada substância.
II .- Quanto maior o calor latente de fusão, tanto
maior o ponto de fusão.
III - É necessário mais calor para fundir um grama
de gelo a 0 °C do que um grama de chumbo a 327 °C.
Quais estão corretas?
(A) Apenas I
(B) Apenas II
(C) Apenas I e III
(D) Apenas II e III
(E) I, II e III
32. (UFRGS) Se a massa e a temperatura
de um gás contido em um recipiente não variam enquanto o volume é duplicado, a
densidade do gás
(A) reduz-se à metade.
(B) reduz-se a um quarto do valor inicial.
(C) permanece constante.
(D) duplica.
(E) quadruplica.
33. (UFRGS) Para que possa haver transferência de
energia na forma de calor entre dois corpos em contato é suficiente que exista
entre eles uma diferença de
(A) temperatura
(B) massa
(C) calor
(D) energia interna
(E) energia cinética de translação
34. (UFRGS) Assinale a alternativa que completa
corretamente as lacunas do seguinte texto:
À pressão atmosférica, nitrogênio líquido entra em
ebulição a uma temperatura de -196°C . Um grama de nitrogênio líquido, a essa
temperatura, comparado com um grama de vapor de nitrogênio, também a -196°C, possui ....... energia. À pressão atmosférica, o ponto de solidificação do mercúrio é -39°C. Quando uma certa quantidade de mercúrio líquido a -39°C é colocada em nitrogênio líquido a -196°C, entra em ebulição o .......... e começa a solidificar o .......... .
(A) mais - mercúrio - nitrogênio
(B) mais - nitrogênio - mercúrio
(C) a mesma - nitrogênio - mercúrio
(D) menos - mercúrio - nitrogênio
(E) menos - nitrogênio - mercúrio
35. (UFRGS) Tanto energia cinética de translação
quanto energia interna podem ser transferidas de um corpo (ou sistema) para
outro. Essa energia transferida é entendida como um processo, o qual só tem
significado físico enquanto estiver ocorrendo. São exemplos de processos de
transferência de energia:
(A) calor e trabalho
(B) massa e carga elétrica
(C) trabalho e massa
(D) calor e massa
(E) calor e carga elétrica
36. (UFRGS) O diagrama representa a pressão p em
função do volume V de um gás ideal. Analisando o diagrama, em qual dos
processos o gás NÃO sofreu variação de temperatura? (A) De A para B
(B) De B para C
(C) De C para D
(D) De D para E
(E) De E para A
37. (UFRGS) Com 336 kJ de energia pode-se,
aproximadamente,
I - fundir ......... kg de gelo a zero °C.
II - elevar a temperatura de 1 kg de água de 20°C para ..........°C.
III - evaporar .......... kg de água a 100°C.
Dados: Calor de fusão do gelo: 336 J/g.
Calor específico da água: 4,UFRGS/19 J/g
°C .
Calor de vaporização da água: 2268 J/g.
Assinale a alternativa que preenche de forma
correta as três lacunas, respectivamente.
(A) 1 / 100 / 6,75
(B) 1000 / 80 / 0,15
(C) 1 / 80 / 0,15
(D) 1000 / 100 / 6,75
(E) 1 / 100 / 0,15
38.(UFRGS) No interior de uma geladeira, a
temperatura é aproximadamente a mesma em todos os pontos graças à circulação do
ar. O processo de transferência de energia causado por essa circulação de ar é
denominado
(A) radiação
(B) convecção
(C) condução
(D) compressão
(E) reflexão
39. Na figura estão esquematizados os componentes
básicos de uma geladeira. Na tubulação ligada ao compressor 2 circula um gás
que alternadamente se vaporiza e se liquefaz e, deste modo, transfere energia.

Para que a transferência de energia se dê de dentro
para fora da geladeira, em quais pontos do esquema devem ocorrer,
respectivamente, a vaporização e a liquefação do gás?
(A) 3 e 4
(B) 1 e 3
(C) 4 e 1
(D) 3 e 1
(E) 4 e 3
40. (UFRGS) Um termômetro está à temperatura
ambiente. O que ocorre com este termômetro quando ele é introduzido em um
líquido com temperatura superior à do ambiente?
(A) Aumenta sua energia interna mas sua temperatura
permanece constante.
(B) Aumenta sua temperatura mas sua energia interna
permanece constante.
(C) Sua energia interna e sua temperatura aumentam.
(D) Aumenta sua temperatura mas diminui sua energia
interna.
(E) Aumenta o calor do termômetro mas
sua energia interna diminui.
41. (UFRGS) A água contida em uma bacia é colocada
ao ar livre para evaporar. Qual das alternativas indica um processo que
contribui para reduzir a quantidade de água evaporada por unidade de tempo?
(A) Aumento da pressão atmosférica.
(B) Redução da umidade relativa do ar.
(C) Aumento da intensidade do vento.
(D) Aumento da temperatura da água.
(E) Mudança da água para uma bacia de
diâmetro maior.
42. (UFRGS) Assinale a alternativa que preenche
corretamente as lacunas do texto abaixo.
A função do compressor de uma geladeira é a de
aumentar a pressão sobre o gás freon contido na tubulação. Devido à rapidez com
que ocorre a compressão, esta pode ser considerada uma transformação .........
.
A temperatura e a pressão do gás se elevam. Como
não há trocas de calor, o trabalho realizado pelo compressor é igual à variação
da
energia ......... do gás.
(A) adiabática - interna
(B) isotérmica - cinética
(C) isotérmica - interna
(D) adiabática - potencial
(E) isobárica - interna
43. (UFRGS) Os pontos A, B e C do gráfico pressão
p em função do volume V na figura indicam três estados de uma mesma amostra de
um gás perfeito.

Unidades arbitrárias de p e V.
Sendo TA, TB e TC as temperaturas absolutas correspondentes aos referidos estados, podemos
afirmar que
(A) TC > TB > TA
(B) TC = TB > TA
(C) TC = TB = TA
(D) TC < TB = TA
(E) TC > TB = TA
44. (UFRGS) A chama de um bico de Bunsen libera 16
kJ de energia por minuto. A energia é toda transferida à massa de 0,3 kg de um líquido cujo calor específico é 2,4 kJ/kg °C . Sabendo-se que o ponto de ebulição desse
líquido é 80 °C, quanto tempo transcorre, aproximadamente, até que sua
temperatura se eleve de 32 °C até o ponto de ebulição?
(A) 1296 s
(B) 130 s
(C) 13 s
(D) 2,16 s
(E) 0,13 s
45. (UFRGS) A maioria dos corpos aumenta de volume
quando recebe energia transferida por diferença de temperatura.
Qual das alternativas refere-se a um processo que
isso NÃO acontece?
(A) Água é aquecida de 20°C a 70°C.
(B) Gelo no ponto de fusão (0°C) é aquecido e se funde.
(C) O mercúrio de um termômetro é aquecido de 20°C a 70°C.
(D) Mercúrio sólido no ponto de fusão (-39°C) é aquecido e se funde.
(E) Um bloco de alumínio é aquecido de 20°C a 70°C.
46. (UFRGS) O fato de barras de ferro contidas em
uma viga de concreto não provocarem rachaduras no concreto explica-se pela
semelhança que existe entre os valores do
(A) calor específico desses materiais.
(B) calor de fusão desses materiais.
(C) coeficiente de condutividade térmica desses
materiais.
(D) coeficiente de dilatação linear desses
materiais.
(E) coeficiente de atrito desses
materiais.
47. (UFRGS) Uma massa m de gás é aquecida a
volume constante. A variação DU da
energia interna desse gás é igual(A) ao calor Q que foi transferido para ele.
(B) ao trabalho W realizado sobre ele.
(C) ao produto da pressão inicial Pi do gás pelo
seu volume V.
(D) ao produto da pressão final Pf do gás pelo seu
volume V.
(E) a zero.
48. (UFRGS) Uma amostra de uma certa substância,
contida em recipiente aberto, encontra-se inicialmente no estado sólido a uma
temperatura To. Uma quantidade total de energia Qtot é,
então, transferida para a amostra na forma de calor. O gráfico representa
qualitativamente (portanto não em escala) as variações de temperatura ocorridas
durante a transferência térmica.
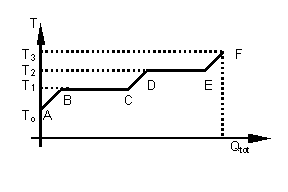
Podemos, então, concluir que
(A) no trecho AB a substância está sofrendo uma
mudança de fase.
(B) no trecho BC a substância toda encontra-se no
estado líquido.
(C) nos trechos BC e DE nenhum calor foi
transferido para a substância.
(D) no trecho DE parte da substância encontra-se no
estado sólido.
(E) no trecho DE parte da substância
encontra-se no estado gasoso.
49. (UFRGS) Em um recipiente fechado, misturam-se
duas porções iguais de água com capacidade térmica de 2 kJ/°C cada e a
temperaturas iniciais diferentes. Se não ocorresse transferência de energia
para o recipiente e para o meio, a temperatura de equilíbrio da mistura seria 30°C, mas foi de 28°C. Quanta energia foi transferida da água para a sua vizinhança, na forma de
calor?
(A) 4 kJ.
(B) 8 kJ.
(C) 20 kJ.
(D) 56 kJ.
(E) 60 kJ.
50. (UFRGS) Qual das afirmações abaixo não está correta?
(A) Diferença de temperatura é a condição para
transferência de energia na forma de calor entre corpos em contato.
(B) Geralmente materiais adequados para manter
elevada a temperatura de um corpo são próprios para mantê-la baixa.
(C) Num sistema termodinâmico que sofre uma
transformação adiabática, a temperatura se mantém constante.
(D) A temperatura absoluta de um gás ideal é
proporcional à energia cinética média associada ao movimento microscópico de
suas partículas.
(E) Quando é mantida constante a
temperatura do gás ideal contido em um recipiente hermeticamente fechado, o
produto de seu volume por sua pressão é constante.
51. (UFRGS) Um gás realiza o ciclo termodinâmico
representado no diagrama p-V da figura, onde A é o ponto correspondente ao
estado termodinâmico inicial do gás.
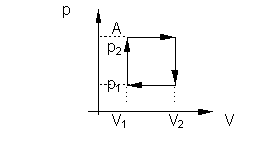
O calor transferido para o gás durante o ciclo
completo é igual a
(A) zero.
(B) p1(V2 - V1).
(C) p2(V2 - V1).
(D) (p2 - p1)(V2 -
V1).
(E) (p2 + p1)(V2 - V1)/2.
52. (UFRGS) Analise cada uma das afirmações e
indique se é verdadeira (V) ou falsa (F):
( ) A irradiação térmica é o único modo de
propagação de calor no vácuo.
( ) Na condução de calor, a energia propaga-se de
átomo (ou molécula) para átomo (ou molécula).
( ) A convecção é um processo de propagação de
calor que ocorre em qualquer estado da matéria.
Quais são, pela ordem, as indicações corretas?
(A) V - F - F.
(B) F - V - F.
(C) F - F - V.
(D) F - V - V.
(E) V- V - F.
53. (UFRGS) Sobre uma superfície plana de 6 m² incide energia solar à razão de 1000 W/m². Quantos kJ de energia absorve, no máximo, essa
superfície durante um minuto, sabendo-se que apenas 50% da energia incidente é
absorvida por ela?
(A) 18
(B) 36
(C) 180
(D) 360
(E) 1800
54 (UFRGS) Se todo ar fosse retirado do interior
de um recipiente de vidro cheio de esferas, também de vidro, seria possível a
propagação do calor, através dele, apenas por
(A) condução.
(B) radiação.
(C) convecção e radiação.
(D) convecção e condução.
(E) condução e radiação.
55. (UFRGS) O gráfico representa a temperatura T
de um gás ideal em função do volume V.
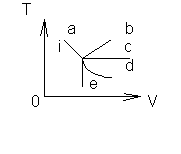
Em que transformação a variação da energia interna
do gás foi nula?
(A) ia
(B) ib
(C) ic
(D) id
(E) ie
56 (UFRGS) Associe o instrumento de medida
(coluna da direita) com a respectiva grandeza física (coluna da esquerda) que
pode ser medida com esse instrumento.
1. calor ( ) termômetro
2. temperatura ( ) amperímetro
3. potência
4. diferença de potencial
5. intensidade de corrente elétrica
A sequência dos números que estabelece as
associações corretas na coluna da direita, quando lida de cima para baixo, é
(A) 1 - 3
(B) 1 - 5
(C) 2 - 4
(D) 2 - 5
(E) 3 - 4
57 (PPCV - UFRGS) O gráfico abaixo representa
a temperatura em função do tempo para dois corpos diferentes. Durante o tempo t1,
ambos receberam a mesma quantidade de calor.
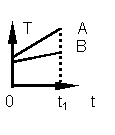
A partir do gráfico pode-se afirmar que
(A) o corpo A sofreu menor variação de temperatura
que o corpo B durante o tempo t1.
(B) o corpo B tem necessariamente maior massa que o
corpo A .
(C) a capacidade térmica do corpo A é maior que a
do corpo B .
(D) a capacidade térmica do corpo B é maior que a
do corpo A .
(E) ambos têm a mesma capacidade
térmica.
58 (PPCV - UFRGS) Uma certa massa de
gás ideal possui um volume V. Para duplicar o volume do gás deve-se:
I - duplicar sua temperatura absoluta, mantendo
constante sua pressão.
II - duplicar sua pressão e duplicar sua
temperatura absoluta.
III - manter sua temperatura absoluta constante e
reduzir sua pressão pela metade.
Quais das alternativas estão corretas
(A) Apenas I.
(B) Apenas II.
(C) Apenas III.
(D) Apenas I e III.
(E) Apenas II e III.
59. (PPCV - UFRGS) Sobre uma barra de
gelo de 10 kg, à temperatura de 0°C, é colocado um bloco de ferro de 400 g a 80°C. Qual a quantidade de gelo que irá derreter-se ao entrar em contato com o bloco de
ferro?
Suponha que haja troca de calor somente
entre o gelo e o ferro. (cferro = 0,113 cal/g°C )
60. (PPCV - UFRGS) Uma certa massa de
gás ideal sofreu uma transformação isobárica, alterando seu volume de 1,0 m³ para 0,4 m³. Neste processo o gás cedeu 100 J ao meio exterior e essa transformação efetuou-se
a uma pressão constante de 30 N/m².
a) Qual o trabalho realizado sobre o sistema?
b) Qual a variação da energia interna do
gás no processo?
61. (UFRGS) Para que dois corpos possam trocar calor
é necessário que
I - estejam a diferentes temperaturas.
II - tenham massas diferentes.
III - exista um meio condutor de calor entre eles.
Quais são as afirmações corretas?
(A) Apenas I.
(B) Apenas II.
(C) Apenas I e II.
(D) Apenas I e III.
(E) I, II e III.
62. (UFRGS) Um cubo de gelo com massa de 2 kg, já na temperatura de fusão da água, está inicialmente em repouso a 10 m acima de uma superfície rígida. Ele cai livremente e se choca com esta superfície. Qual é,
aproximadamente, a máxima massa de gelo que pode se fundir nesse processo?
Dados: Calor de fusão do gelo = 80 cal/g; 1 cal = 4,18 J; aceleração
gravitacional = 10 m/s².
(A) 0,2 g
(B) 0,6 g
(C) 1,0 g
(D) 1,2 g
(E) 1,5 g
63. (UFRGS) Um recipiente de vidro, cujas paredes
são finas, contém glicerina. O conjunto se encontra a 20°C. O coeficiente de dilatação linear do vidro é 27x10-6 °C-1 e o coeficiente
de dilatação volumétrica da glicerina é 5,0x10-4 °C-1. Se
a temperatura do conjunto se elevar para 60°C, pode-se afirmar que o nível da glicerina no recipiente
(A) baixa, porque a glicerina sofre um aumento de
volume menor do que o aumento na capacidade do recipiente.
(B) se eleva, porque a glicerina aumenta de volume
e a capacidade do recipiente diminui de volume.
(C) se eleva, porque apenas a glicerina aumenta de
volume.
(D) se eleva, apesar da capacidade do recipiente
aumentar.
(E) permanece inalterado, pois a
capacidade do recipiente aumenta tanto quanto o volume de glicerina.
64. (UFRGS) A figura, abaixo, representa um
recipiente cilíndrico com um êmbolo, ambos feitos de material isolante térmico.
Não existe atrito entre o êmbolo e as paredes do cilindro. Pendurado ao êmbolo,
em equilíbrio, há um corpo suspenso por um fio. No interior do cilindro, há uma
amostra de gás ideal ocupando um volume de 5 litros, à temperatura de 300 K e à
pressão de 0,6 atm. Em um dado momento o fio é cortado.
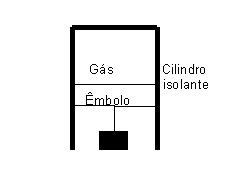
Quando novamente o gás se encontrar em equilíbrio
termodinâmico, qual será o seu volume (V), a sua pressão (p) e a sua
temperatura (T)?
(A) V > 5 litros, p > 0,6 atm, T = 300 K
(B) V < 5 litros, p > 0,6 atm, T > 300 K
(C) V < 5 litros, p > 0,6 atm, T = 300 K
(D) V < 5 litros, p = 0,6 atm, T = 300 K
(E) V > 5 litros, p < 0,6 atm, T
> 300 K
GABARITO
| 0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
|
| 0 |
D |
A |
D |
C |
E |
A |
D |
D |
E |
|
| 1 |
C |
E |
E |
D |
E |
B |
E |
D |
B |
B |
| 2 |
D |
D |
A |
E |
* |
B |
D |
E |
C |
A |
| 3 |
D |
C |
A |
A |
E |
A |
B |
E |
B |
B |
| 4 |
C |
A |
A |
B |
B |
B |
D |
A |
E |
B |
| 5 |
C |
D |
E |
C |
B |
C |
D |
D |
D |
** |
| 6 |
# |
A |
B |
D |
B |